Nuolat tobulėjant molekulinės biologijos technologijoms, ryšys tarp genų mutacijų ir defektų bei ligų įgauna vis išsamesnį supratimą.Nukleino rūgštys susilaukė daug dėmesio dėl didelio jų taikymo diagnozuojant ir gydant ligas.Nukleino rūgščių vaistai reiškia dirbtinai susintetintus DNR arba RNR fragmentus, turinčius ligos gydymo funkcijų.Tokie vaistai gali tiesiogiai veikti ligas sukeliančius tikslinius genus arba ligas sukeliančius tikslinius mRNR ir atlikti vaidmenį gydant ligas genų lygmeniu.Palyginti su tradiciniais mažų molekulių vaistais ir antikūnų vaistais, nukleino rūgščių vaistai gali reguliuoti ligą sukeliančių genų ekspresiją nuo šaknų ir turi „simptomų gydymo ir pagrindinės priežasties gydymo“ savybes.Nukleino rūgšties vaistai taip pat turi akivaizdžių pranašumų, tokių kaip didelis efektyvumas, mažas toksiškumas ir didelis specifiškumas.Nuo 1998 m., kai buvo išleistas pirmasis nukleorūgščių preparatas fomivirseno natrio druska, daugelis nukleorūgščių vaistų buvo patvirtinti klinikiniam gydymui.
Šiuo metu pasaulyje parduodami nukleino rūgščių vaistai daugiausia apima antisensinę nukleino rūgštį (ASO), mažą interferuojančią RNR (siRNR) ir nukleorūgščių aptamerius.Išskyrus nukleorūgščių aptamerius (kurie gali viršyti 30 nukleotidų), nukleorūgščių vaistai paprastai yra oligonukleotidai, sudaryti iš 12–30 nukleotidų, taip pat žinomi kaip oligonukleotidiniai vaistai.Be to, miRNR, ribozimai ir dezoksiribozimai taip pat parodė didelę vystymosi vertę gydant įvairias ligas.Nukleino rūgščių vaistai šiandien tapo viena perspektyviausių biomedicinos tyrimų ir plėtros sričių.
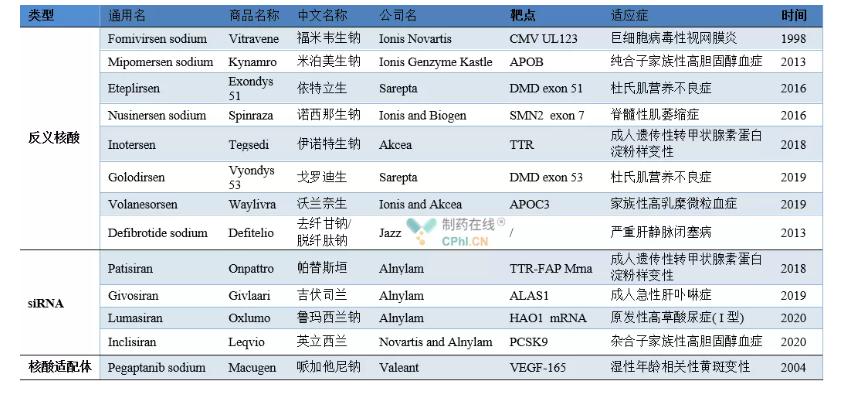
Patvirtintų vaistų nuo nukleino rūgščių pavyzdžiai
Antisensinė nukleorūgštis
Antisense technologija yra nauja vaistų kūrimo technologija, pagrįsta Watson-Crick bazės papildymo principu, naudojant specifinius papildomus DNR arba RNR fragmentus, kuriuos dirbtinai susintetina arba susintetina organizmas, siekiant specifiškai reguliuoti tikslinių genų ekspresiją.Antisensinė nukleorūgštis turi bazinę seką, kuri yra komplementari su tiksline RNR ir gali specifiškai prie jos prisijungti.Antisensinės nukleorūgštys paprastai apima antisensinę DNR, antisensinę RNR ir ribozimus.Tarp jų, dėl didelio stabilumo ir mažos antisensinės DNR kainos, antisensinė DNR užima dominuojančią vietą dabartiniuose antisensinių nukleorūgščių vaistų tyrimuose ir taikyme.
Fomivirseno natrio druską (prekinį pavadinimą Vitravene) sukūrė Ionis Novartis.1998 m. rugpjūčio mėn. FDA jį patvirtino citomegalovirusinio retinito gydymui pacientams, kurių imuninė sistema susilpnėjusi (daugiausia AIDS sergantiems pacientams), ir tapo pirmuoju nukleino rūgščių vaistu, kuris buvo parduodamas.Fomivirsenas slopina dalinę CMV baltymų ekspresiją, prisijungdamas prie specifinės mRNR (IE2), taip reguliuodamas viruso genų ekspresiją, kad būtų pasiektas terapinis poveikis.Tačiau dėl didelio efektyvumo antiretrovirusinio gydymo atsiradimo, kuris labai sumažino pacientų skaičių, 2002 ir 2006 metais „Novartis“ panaikino Fomivirsen vaistų rinkodaros leidimą atitinkamai Europoje ir JAV, o preparato pateikimas į rinką buvo sustabdytas.
Mipomerseno natrio druska (prekinis pavadinimas Kynamro) yra ASO vaistas, kurį sukūrė prancūzų kompanija Genzyme.2013 m. sausio mėn. FDA jį patvirtino homozigotinės šeiminės hipercholesterolemijos gydymui.Mipomersenas slopina ApoB-100 baltymo (apolipoproteino) ekspresiją, prisijungdamas prie ApoB-100mRNR, taip žymiai sumažindamas žmogaus mažo tankio lipoproteinų cholesterolio, mažo tankio lipoproteinų kiekį ir kitus rodiklius, tačiau dėl šalutinio poveikio, pvz., toksinio poveikio kepenims, 2012 m. gruodžio 13 d.
2016 m. rugsėjo mėn. Eteplirsen (prekinis pavadinimas Exon 51), kurį Sarepta sukūrė Diušeno raumenų distrofijai (DMD) gydyti, buvo patvirtintas FDA.DMD pacientai paprastai negali išreikšti funkcinio antiatrofinio baltymo dėl DMD geno mutacijų organizme.Eteplirsenas specifiškai jungiasi prie baltymo išankstinės pasiuntinio RNR (Pre-mRNR) 51 egzono, pašalina 51 egzoną ir atkuria kai kuriuos pasroviui esančius genus.
Nusinersen yra ASO vaistas, sukurtas Spinraza, skirtas stuburo raumenų atrofijai gydyti ir buvo patvirtintas FDA 2016 m. gruodžio 23 d. 2018 m. Tegsedi sukurtas Inotesen, skirtas suaugusiųjų paveldimoms transtiretino amiloidozei gydyti, buvo patvirtintas FDA.2019 m. FDA patvirtino Golodirsen, kurį Sarepta sukūrė Diušeno raumenų distrofijai gydyti.Jo veikimo mechanizmas toks pat kaip ir Eteplirsen, o jo veikimo vieta tampa 53 egzonu. Tais pačiais metais Ionisand Akcea bendrai sukurtas šeiminės hiperchilomikronemijos gydymas buvo patvirtintas Europos vaistų agentūros (EMA).Volanesorsenas reguliuoja trigliceridų metabolizmą, slopindamas apolipoproteino C-Ⅲ gamybą, tačiau jis taip pat turi šalutinį poveikį – mažina trombocitų kiekį.
Defibrotidas yra plazmino savybių turintis oligonukleotidų mišinys, kurį sukūrė Jazz.Jame yra 90% viengrandžių DNR ir 10% dvigrandžių DNR.Jį EMA patvirtino 2013 m., o vėliau FDA patvirtino sunkių kepenų venų gydymui.Okluzinė liga.Defibrotidas gali padidinti plazmino aktyvumą, padidinti plazminogeno aktyvatorių, skatinti trombomodulino reguliavimą ir sumažinti von Willebrand faktoriaus bei plazminogeno aktyvatoriaus inhibitorių ekspresiją, kad būtų pasiektas terapinis poveikis.
siRNR
siRNR yra nedidelis specifinio ilgio ir sekos RNR fragmentas, gaunamas pjaunant tikslinę RNR.Šios siRNR gali specifiškai sukelti tikslinės mRNR degradaciją ir pasiekti genų nutildymo poveikį.Palyginti su cheminiais mažų molekulių vaistais, siRNR vaistų genų slopinimo poveikis yra labai specifiškas ir efektyvus.
2018 m. rugpjūčio 11 d. pirmasis siRNA vaistas patisiran (prekinis pavadinimas Onpattro) buvo patvirtintas FDA ir oficialiai išleistas.Tai vienas iš pagrindinių etapų RNR trukdžių technologijos vystymosi istorijoje.Patisiran bendrai sukūrė Alnylam ir Genzyme, Sanofi dukterinė įmonė.Tai siRNR vaistas, skirtas paveldimos tiroksino sukeltos amiloidozės gydymui.2019 m. FDA patvirtino givosiraną (prekinį pavadinimą Givlaari) kaip antrąjį siRNR vaistą, skirtą suaugusiųjų ūminei kepenų porfirijai gydyti.2020 metais Alnylam sukūrė pirminį I tipo vaistą, skirtą vaikų ir suaugusiųjų gydymui.FDA patvirtino Lumasiraną su dideliu oksalurija.2020 m. gruodžio mėn. EMA patvirtino Inclisiran, kurį bendrai sukūrė Novartis ir Alnylam suaugusiųjų hipercholesterolemijai arba mišriai dislipidemijai gydyti.
Aptamer
Nukleino rūgščių aptamerai yra oligonukleotidai, galintys prisijungti prie įvairių tikslinių molekulių, tokių kaip mažos organinės molekulės, DNR, RNR, polipeptidai arba baltymai, turintys didelį afinitetą ir specifiškumą.Palyginti su antikūnais, nukleino rūgščių aptamerams būdingos paprastos sintezės, mažesnės sąnaudos ir platus taikinių spektras bei platesnis vaistų taikymo ligų diagnostikos, gydymo ir profilaktikos potencialas.
Pegaptanibas yra pirmasis Valeant sukurtas nukleino rūgšties aptamero vaistas, skirtas šlapiai su amžiumi susijusiai geltonosios dėmės degeneracijai gydyti ir 2004 m. buvo patvirtintas FDA. Vėliau 2006 m. sausio mėn. ir 2008 m. liepos mėn. jį patvirtino EMA ir PMDA, ir jis buvo išleistas į rinką.Pegaptanibas slopina angiogenezę derindamas erdvinę struktūrą ir kraujagyslių endotelio augimo faktorių, kad pasiektų gydomąjį poveikį.Nuo tada ji susidūrė su panašių vaistų „Lucentis“ konkurencija, o jos rinkos dalis labai sumažėjo.
Nukleino rūgščių vaistai tapo karšta vieta klinikinių vaistų ir naujų vaistų rinkoje dėl jų nepaprasto gydomojo poveikio ir trumpo vystymosi ciklo.Kaip naujas narkotikas, jis susiduria su iššūkiais ir susiduria su galimybėmis.Dėl savo egzogeninių savybių nukleorūgščių specifiškumas, stabilumas ir efektyvus pristatymas tapo pagrindiniais kriterijais, sprendžiant, ar oligonukleotidai gali tapti labai efektyviais nukleorūgščių vaistais.Netikslinis poveikis visada buvo pagrindinis nukleino rūgščių vaistų aspektas, kurio negalima ignoruoti.Tačiau nukleino rūgščių vaistai gali paveikti ligą sukeliančių genų ekspresiją nuo šaknų ir gali pasiekti sekos specifiškumą vienos bazės lygmeniu, o tai turi „pagrindinės priežasties ir simptomų gydymo“ ypatybes.Atsižvelgiant į vis daugiau ligų kintamumą, tik genetinis gydymas gali pasiekti ilgalaikių rezultatų.Nuolat tobulėjant, tobulėjant ir progresuojant susijusioms technologijoms, nukleino rūgščių vaistai, atstovaujami antisensinių nukleino rūgščių, siRNR ir nukleorūgščių aptamerų, neabejotinai sukels naują bangą ligų gydymo ir farmacijos pramonėje.
Rnuorodos:
[1] Liu Shaojin, Feng Xuejiao, Wang Junshu, Xiao Zhengqiang, Cheng Pingsheng.Nukleino rūgščių vaistų rinkos analizė mano šalyje ir atsakomosios priemonės[J].Kinijos biologinės inžinerijos žurnalas, 2021, 41(07): 99–109.
[2] Chen Wenfei, Wu Fuhua, Zhang Zhirong, Sun Xun.Parduodamų nukleino rūgščių vaistų farmakologijos tyrimų pažanga[J].Chinese Journal of Pharmaceuticals, 2020, 51 (12): 1487–1496.
[3] Wang Jun, Wang Lan, Lu Jiazhen, Huang Zhen.Parduodamų nukleorūgščių vaistų veiksmingumo ir tyrimų eigos analizė[J].Kinijos naujų vaistų žurnalas, 2019, 28(18): 2217-2224.
Apie autorių: Sha Luo, kinų medicinos tyrimų ir plėtros darbuotojas, šiuo metu dirba didelėje vietinėje vaistų tyrimų ir plėtros įmonėje ir yra įsipareigojęs tirti ir kurti naujus kiniškus vaistus.
Susiję produktai:
Paskelbimo laikas: 2021-11-19